| 제목 | 구강면역 3. 왜 입속상처는 잘 아물까? | ||||
|---|---|---|---|---|---|
| 작성자 | 닥스메디 | 등록일 | 2022.12.20 | 조회수 | 109359 |
|
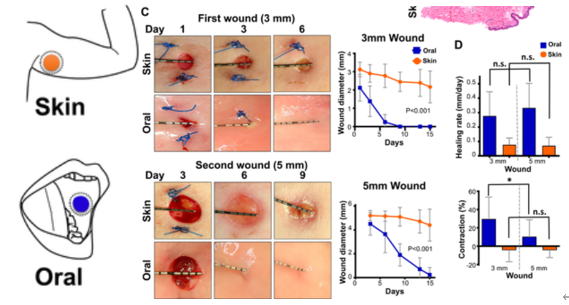
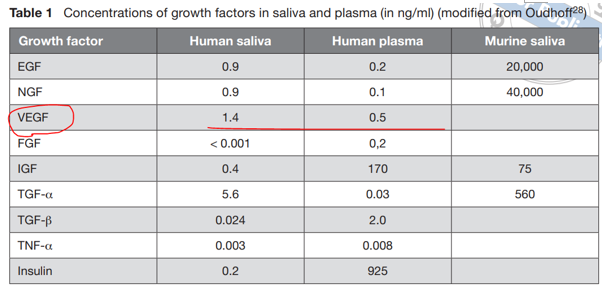
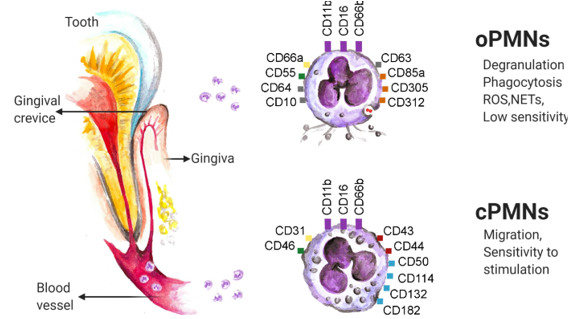
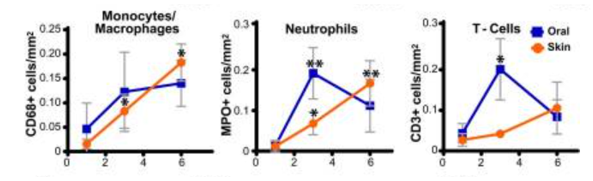
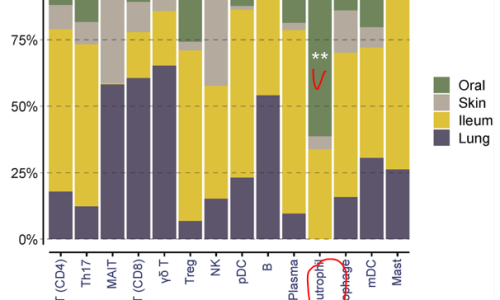
1. 타액 A. 타액은 일단 상처를 적혀준다. 피부에 상처가 나면 습윤밴드를 붙이면 빨리 아문다. 입속은 타액 덕에 그 자체로 촉촉하다. B. 타액은 피부나 구강조직을 아물게 하는 섬유아세포(fibroblast)와 상피세포들의 증식을 빠르게 한다. (Rodrigues Neves, Buskermolen et al. 2019) C. 타액 속 성장인자가 치유 촉진을 돕는다. 혈액만이 아니라, 타액에도 상당한 성장인자기 있는데, 그중에서도 특히 VEGF 란 성장인자는 오히려 혈액보다 타액에서도 훨씬 더 농도가 높다. (Brand, Ligtenberg et al. 2014) D. 히스타틴(hystatin) 같은 치유 촉진 단백질 2. 구강 조직 속 면역세포들의 조절 능력 A. 원래 구강에 많은 중성구를 포함한 면역세포들은 많다. 대표적으로 중성구는 혈액에서 직접 빠져나와 치주포켓을 늘 순찰하고 있어서, 구강에는 늘 100만 개 이상의 중성구들이 상주한다 B. 그리고, 구강의 중성구는 혈액 속 중성구와는 다른 특성을 갖는다. 구강의 중성구는 혈액의 중성구에 비해 수명이 다 한 후에도 TNF 같은 사이토카인이 이제 그만 자살(apoptosis)라는 신호를 줘도 이에 덜 민감하게 반응하며 수명을 연장할 수 있다. (Domnich, Riedesel et al. 2020) C. 구강이든 상처가 나면 일정한 염증 과정이 중간이 있을 수밖에 없다. 그런데, 구강의 중성구를 포함한 면역세포들은 치유 초기엔 기능이 활성화되었다가 며칠 후엔 스스로 자제함으로써 과한 염증을 예방한다. (Iglesias-Bartolome, Uchiyama et al. 2018) 3. 여러 세포들 간 촘촘한 네트워크 A. 상처가 아무는 데는 섬유아세포나 상피세포를 포함한 여러 세포들의 역할 덕이고, 이런 세포들을 만들어 낼 수 있는 기질세포(Mesenchymal Stromal Cell) 의 역할이 중요하다. B. 구강조직에 늘 상주하던 중성구는 상처가 나면, 자신이 먼저 달려감과 동시에, 신호물질을 뿌려서 여러 세포들에 신호를 보낸다. 그러면 다른 면역세포들과 기질세포들도 긴장하여 상처치유에 나선다. C. 그중에서도 특히 중성구와 기질세포의 연결축(neutrophil stromal cell axis) 이 튼튼한 것으로 보인다. (Williams, Greenwell-Wild et al. 2021) 4. 마이크로바이옴 A. 타액과 치주포켓 속에는 현재 774 종에 달하는 입속세균들이 상주해 있다. 그리고, 그런 세균들은 이미 항균물질과 중성구를 품고 있는 타액과 구강환경에 적응되고 공진화해온 녀석들이다. 이들 공존세균들이 구강의 상처치유를 돕는 것은 자신들의 생존에도 유리하다. B. 실제 공진화 세균인 프로바이오틱스 유산균을 이용해 상처치유를 촉진한 예가 있다. (Han, Jia et al. 2020) 대표적 구강유해균인 진지발리스가 과증식해 구강 내 세균의 균형이 깨지면 심지어 mesenchymal stem cell (MSC) 의 증식이 손상되기도 하는데, 구강유산균으로 도 쓰이는 락토바실러스가 그 불균형을 해소하여 상처치유를 촉진시켜 줄 수 있다는 것이다.
Brand, H. S., A. J. Ligtenberg, E. C. J. S. s. Veerman and functions (2014). "Saliva and wound healing." 24: 52-60. Domnich, M., J. Riedesel, E. Pylaeva, C. H. Kürten, J. Buer, S. Lang and J. J. F. i. I. Jablonska (2020). "Oral neutrophils: Underestimated players in oral cancer." 11: 565683. Han, N., L. Jia, L. Guo, Y. Su, Z. Luo, J. Du, S. Mei and Y. Liu (2020). "Balanced oral pathogenic bacteria and probiotics promoted wound healing via maintaining mesenchymal stem cell homeostasis." Stem Cell Research & Therapy 11(1): 61. Iglesias-Bartolome, R., A. Uchiyama, A. A. Molinolo, L. Abusleme, S. R. Brooks, J. L. Callejas-Valera, D. Edwards, C. Doci, M. L. Asselin-Labat, M. W. Onaitis, N. M. Moutsopoulos, J. S. Gutkind and M. I. Morasso (2018). "Transcriptional signature primes human oral mucosa for rapid wound healing." Sci Transl Med 10(451). Rodrigues Neves, C., J. Buskermolen, S. Roffel, T. Waaijman, M. Thon, E. Veerman and S. Gibbs (2019). "Human saliva stimulates skin and oral wound healing in vitro." 13(6): 1079-1092. Williams, D. W., T. Greenwell-Wild, L. Brenchley, N. Dutzan, A. Overmiller, A. P. Sawaya, S. Webb, D. Martin, G. Hajishengallis, K. Divaris, M. Morasso, M. Haniffa and N. M. Moutsopoulos (2021). "Human oral mucosa cell atlas reveals a stromal-neutrophil axis regulating tissue immunity." Cell 184(15): 4090-4104.e4015.
출처 : 사과나무의료재단 김혜성이사장 블로그
|
|||||